À chaque sortie nature, la question tombe inévitablement : « Comment vous faites pour le pipi de renard sur les plantes ? ». Les participant·e·s ont souvent peur de l’échinococcose, ce mal invisible. En réalité, ce n’est pas l’urine qui est responsable de la transmission, mais les selles. Alors comment ça se passe et qu’est-ce que l’échinococcose concrètement ?
Les zoonoses
L’échinococcose fait partie des zoonoses, ces maladies qui passent de l’animal à l’humain et inversement. Ce n’est pas un phénomène nouveau mais le reflet de notre histoire commune avec le vivant.
Il y a environ 10 000 ans, au Néolithique, débute l’avènement de l’agriculture et la domestication des animaux. Cette révolution a bouleversé notre rapport à la nature : en vivant plus près des animaux, en les élevant et en partageant nos espaces, nous avons intensifié nos contacts.
Cette proximité, essentielle au développement de nos sociétés, a aussi créé de nouvelles voies de transmission pour les microbes et les parasites. Les zoonoses ont ainsi joué un rôle majeur dans l’évolution et l’adaptation de l’humanité à son environnement (Bendrey et al., 2022 ; Stone, 2020 ; Araújo et al., 2013).
Le parasite en question : Echinococcus multilocularis
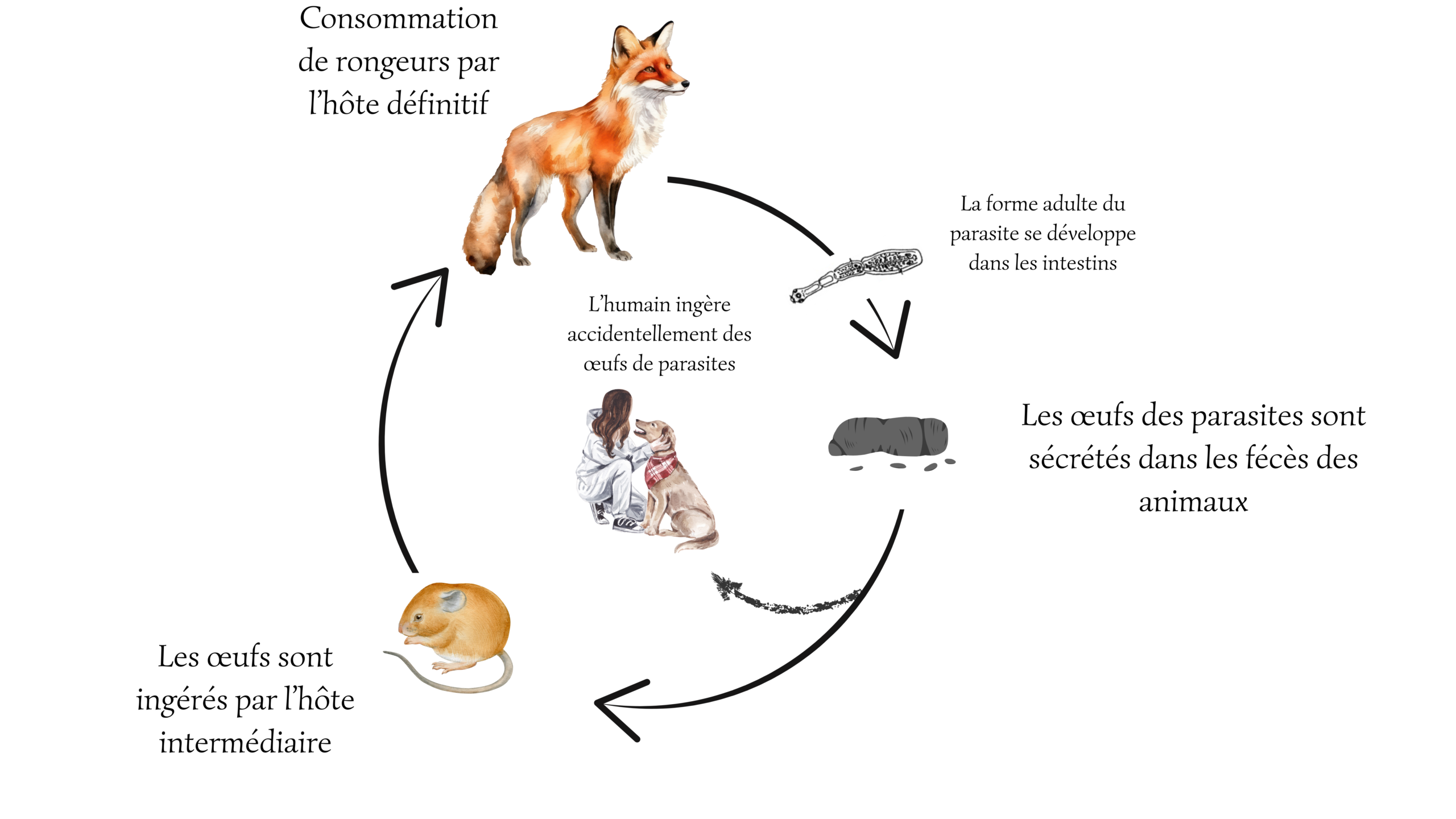
En Suisse et en Europe, on est concerné par l’échinococcose alvéolaire (EA) qui est causée par Echinococcus multilocularis, un petit ver plat de quelques millimètres. Cette infection suit un cycle précis :
- Hôte définitif : Principalement le renard roux (Vulpes vulpes), mais aussi le chien, le chat, le coyote ou le loup selon les régions. C’est dans leur intestin que le ver adulte vit et pond des œufs.
- Hôte intermédiaire : Essentiellement des rongeurs comme le campagnol des champs (Microtus arvalis). Ils ingèrent les œufs, qui se transforment en kystes dans leur foie.
- Hôte accidentel : L’humain. Nous sommes une impasse pour le parasite : nous ingérons les œufs, qui se transforment en kystes dans notre corps, mais nous ne pouvons pas transmettre le parasite à d’autres animaux ou humains (Allemann, 2024).
Le danger réside dans la forme larvaire. Chez l’humain, ces larves forment des kystes qui grossissent lentement, principalement dans le foie, sur une période de 5 à 15 ans (Gottstein et al., 2015).
Symptômes et évolution de l’échinococcose alvéolaire
1. Une maladie invisible au début
- Période d’incubation longue : La maladie reste souvent asymptomatique pendant des années (5 à 15 ans).
- Détection fortuite : Elle est parfois découverte par hasard lors d’un examen médical de routine, avant l’apparition de signes cliniques.
2. Quand les symptômes apparaissent Dans 80% des cas, la maladie est déjà symptomatique au moment du diagnostic. Les signes les plus fréquents sont :
- Douleurs abdominales (souvent dans la partie supérieure droite).
- Ictère (jaunisse de la peau et des yeux), dû à l’obstruction des canaux biliaires.
3. Une évolution lente mais invasive
- Localisation : La lésion se forme principalement dans le foie (97% des cas).
- Comportement : Elle agit comme une tumeur maligne, envahissant progressivement le tissu hépatique, les vaisseaux sanguins et les organes voisins (pancréas, diaphragme).
- Métastases : Dans les cas avancés, le parasite peut se propager à d’autres organes (poumons, rate, cerveau, os). Environ un tiers des patient·e·s présente déjà des signes de propagation au moment du diagnostic.
Comment se transmet la contamination ?
C’est ici que la nuance est cruciale. Contrairement à une idée reçue tenace, la cueillette de plantes sauvages n’est pas le premier facteur de risque. Les études épidémiologiques montrent que la contamination se fait par ingestion d’œufs microscopiques présents dans l’environnement :
- Le contact avec les chiens : C’est souvent le vecteur le plus sous-estimé. Un chien qui chasse des rongeurs ou qui a un comportement de coprophagie (manger des selles) peut ramener des œufs sur son pelage. Le contact physique répété (caresses, léchages) avec un chien non vermifugé dans une zone endémique est une voie majeure de transmission (Cvejic et al., 2016).
- Le contact avec l’environnement : Les œufs sont déposés dans les selles des renards. Ils se retrouvent sur le sol, sur les feuilles basses, ou dans la terre. Le vrai danger réside souvent dans le geste inconscient de porter ses mains à la bouche après avoir manipulé de la terre, des végétaux ou des surfaces contaminées.
- L’eau contaminée : La consommation d’eau non traitée dans des zones endémiques peut aussi être un facteur, bien que moins fréquent en milieu urbain.
La résistance des œufs : Les œufs d’E. multilocularis sont redoutablement résistants. Ils survivent entre -18°C et 27°C, et peuvent résister à 65°C pendant deux heures (Veit et al., 1995 ; Federer et al., 2015). Seule la dessiccation (sécheresse extrême) leur est létale.
Expansion géographique et facteurs de risque
Depuis les années 1990, la répartition du parasite s’est considérablement accrue en Europe, corrélée à l’augmentation des populations de renards liée au succès de la vaccination antirabique (Chautan et al., 2000). En Suisse, environ 30% des renards sont infectés, tant en ville qu’en campagne (Gloor et al., 2001).
Plusieurs facteurs influencent cette expansion :
| Facteur | Impact |
|---|---|
| Changement climatique | Modifie les habitats des hôtes et la survie des œufs |
| Urbanisation des renards | Près de 40% de prévalence dans certaines villes suisses (Deplazes et al., 2004) |
| Modification des paysages | Prairies et pâturages favorisent la transmission |
| Immunodépression | Augmente le risque de développer la maladie (Chauchet et al., 2014) |
En France, les départements les plus touchés sont le Doubs (169 cas en 40 ans), la Haute-Savoie (103 cas), les Vosges (94 cas), la Haute-Saône (70 cas) et le Jura (56 cas) (CNR Échinococcoses, 2022).
Et les plantes sauvages dans tout ça ?
C’est la crainte la plus fréquente, mais les données scientifiques sont rassurantes. Une étude française publiée en 2013 a montré que la cueillette de baies sauvages n’est pas un facteur de risque supplémentaire. En effet, 91% des personnes interrogées (malades comme saines) cueillaient des baies. Si cette activité était dangereuse, on constaterait des milliers de cas chaque année parmi les millions de promeneurs et touristes qui fréquentent les forêts françaises (Piarroux et al., 2013).
Alors, faut-il arrêter de cueillir ? Non, mais il faut adapter nos gestes.
Le risque ne vient pas de la plante en elle-même mais de la contamination de l’environnement immédiat. Voici quelques gestes à garder en tête lors de ta cueillette :
- Récolte en hauteur : Limite les risques de contamination en évitant les plantes au ras du sol ou les rosettes. Les œufs se trouvent principalement sur le sol ou les feuilles basses.
- Observe les traces : Apprends à reconnaître la présence de renards. Leurs excréments sont torsadés, pointus à une extrémité, et contiennent souvent des poils, des ossements ou des graines. Ils sont souvent déposés sur des lieux visibles (pierres, souches, sentiers) pour marquer le territoire.
- Cuis ta récolte : C’est la méthode la plus sûre. Les œufs ne survivent pas à une cuisson de 7,5 à 30 minutes à 70°C. Attention cependant : ils résistent à la congélation à -18°C.
- Hygiène : Il est recommandé de protéger son potager des renards et de se laver systématiquement les mains après avoir manipulé la terre.
Maintenant que tu connais les vrais risques et que tu as les bons réflexes pour te protéger, plus aucune raison de rester à la maison ! N’hésite pas à venir participer à mes ateliers pour apprendre à la découvrir et à la cueillir en toute sérénité.
Références bibliographiques
- Allemann, S. (2024). Thèse de doctorat : Contribution à l’étude de la diversité génétique d’Echinococcus multilocularis. Université de Franche-Comté.
- Araújo, A., et al. (2013). Zoonoses and the Neolithic transition. Journal of Archaeological Science, 40(12), 4789-4798.
- Bendrey, R., et al. (2022). The impact of animal domestication on human health and disease. Evolutionary Anthropology, 31(4), 189-201.
- Chauchet, A., et al. (2014). Increasing incidence of alveolar echinococcosis in France: a 30-year retrospective study. Clinical Infectious Diseases, 59(10), 1433-1440.
- Chautan, M., et al. (2000). Impact of rabies vaccination on fox populations and echinococcosis transmission. Veterinary Research, 31(5), 567-578.
- CNR Échinococcoses. (2022). Rapport annuel de surveillance de l’échinococcose alvéolaire en France. Institut Pasteur.
- Cvejic, M., et al. (2016). Risk factors for human alveolar echinococcosis in Slovenia. Parasites & Vectors, 9, 543.
- Deplazes, P., et al. (2004). Urban foxes and the risk of Echinococcus multilocularis infection in Switzerland. Parasitology International, 53(4), 389-395.
- Federer, M., et al. (2015). Survival of Echinococcus multilocularis eggs under various environmental conditions. International Journal for Parasitology, 45(10), 657-664.
- Gloor, S., Bontadina, F., Hegglin, D., et al. (2001). The rise of urban fox populations in Switzerland. Journal of Mammalian Biology, 66, 155-164.
- Gottstein, B., et al. (2015). Alveolar echinococcosis: from diagnosis to treatment. Current Opinion in Infectious Diseases, 28(5), 456-463.
- Piarroux, M., Piarroux, R., Knapp, J., et al. (2013). Populations at Risk for Alveolar Echinococcosis, France. Emerging Infectious Diseases, 19(5), 786-793.
- Stone, R. (2020). The Neolithic revolution and the rise of infectious diseases. Science, 368(6491), 567-569.
- Veit, P., et al. (1995). Resistance of Echinococcus multilocularis eggs to environmental stress. Parasitology Research, 81(6), 473-477.


